Energía Iónica

- La segunda ionización:
- La tercera ionización:
- Tabla de energia de ionizacion
- Ejemplos de energia de ionizacion
- ¿Qué es la energía de ionización?
- Usos de la energía ionica
- Ventajas y Desventajas de la Energía Iónica
- Energía de ionización ejemplos
- Energía Iónica para niños
- Maquetas del enlace ionico
- Propiedades periodicas de la energia de ionizacion
- Tipos de enlace y electronegatividad
- Características de los enlaces ionicos:
- Como se forman los enlaces ionicos
- Asi se define Electronegatividad
- Variación de las propiedades periódicas de los elementos
- Que son las propiedades periodicas de los elementos
- Calcular energia de ionizacion
- ¿Por que la energia de ionizacion es una propiedad periodica?
- ¿Diferencia entre energía de ionización y potencial de ionizacion?
- Ionización de los átomos
- Imagenes de energia ionica
La energía de ionización también llamada potencial de ionización es la energía que es necesaria para poder separar un electrón en su estado fundamental de un átomo de un átomo de algún elemento que se encuentre en estado gaseoso.
La energía de ionización es equivalente en valor absoluto a la energía con la que el núcleo atómico mantiene unido al electrón: es la energía necesaria para poder ionizar al átomo.
La magnitud de la energía de ionización depende básicamente de tres factores que son fundamentales:
- Radio atómico
- Estructura electrónica de la última capa
- Carga nuclear
El factor determinante sera la configuración electrónica de la última capa, esto es porque cuanto mas estable sea, o mas bien cuanto más se parezca a la de estructura completa, estructura de gas noble, mayor energía necesitara para arrancar un electrón.
Todo lo mencionado anteriormente corresponde la primera ionización. Ahora vamos a ver de que se trata la segunda y la tercera:
La segunda ionización:
Es la necesaria para extraer un electrón de un ion con carga uno.
La tercera ionización:
Esta sería la energía necesaria para poder extraer un electrón de un ion con carga dos, y así sucesivamente.
Tabla de energia de ionizacion
Esta es la tabla periódica de energía de ionización completa:

Ejemplos de energia de ionizacion
Estos son unos ejemplos bastantes prácticos con los que puedes practicar:
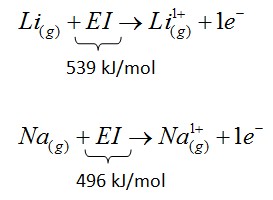
 Energía Eléctrica
Energía Eléctrica¿Qué es la energía de ionización?
Los átomos y las moléculas tienen una medida llamada energía de ionización, que simplemente significa la cantidad de energía requerida para eliminar un electrón mientras esa sustancia se encuentra en estado gaseoso. Este término solía llamarse potencial de ionización, pero ya no se usa. Este IE siempre se mide comenzando con una capa externa, moviéndose hacia adentro hacia el núcleo.
Curiosamente, a medida que los electrones se eliminan de un átomo, se vuelve más difícil eliminar más electrones y requiere más energía de ionización, ya que la carga del átomo ahora ha cambiado.
Existen diferentes unidades utilizadas para medir el IE, dependiendo del campo de la ciencia involucrado. En física, el IE se mide en voltios de electrones (eV) y se refiere a mover un solo electrón. Sin embargo, en química, la IE se mide como la cantidad molar, que se especifica como unidades de kJ / mol o kcal / mol. Esa es la cantidad de energía que toma para que todos los átomos en un mol de una sustancia pierdan un electrón.
Usos de la energía ionica
- Control de rayos: la potencia que se consigue con la ionización permite el control de la fuerza o energía que liberan los rayos en una tormenta, de modo que la intensidad de estos se puede reducir con aparatos específicos que utilizan la mencionada ionización y que están actualmente en desarrollo.
- Biotecnología: la energía de ionización es aplicada para el análisis de proteínas, péptidos, oligonucleótidos.
- Esterilización: Gracias a la ionización es también posible esterilizar un instrumento, de modo que desaparecerán todos los microorganismos de un determinado lugar a través de aplicar un proceso que tiene que ver además con la radiación.
- Detección de amenazas: La energía iónica ha permitido desarrollar métodos que permiten poder detectar cualquier tipo de amenaza que tiene que ver con explosivos y drogas.
- Análisis farmacéutico: Se utiliza para el descubrimiento de drogas, química combinatoria, y para controlar el metabolismo de los medicamentos.
- Tubos fluorescentes y televisores: El proceso de ionización también se da para el buen funcionamineto de los tubos fluorescentes, pero no solo eso sino que también nos sirve para que los televisores de plasma puedan encenderse.
Ventajas y Desventajas de la Energía Iónica
Ventajas de la energía iónica
- Facilidad de creación: Para generar energía iónica no es necesario el uso de la electricidad, solo necesita de electrones y átomos y no es necesario que estos los tome de ahí. De modo que en principio podría llegar a ser una energía limpia si tenemos en cuenta que podría crearse a partir de electrones y átomos tomados de la energía solar con el uso de paneles solares.
- Ahorro de Energía: Algunas misiones espaciales, utilizan un sistema de motores iónicos (similares aunque evolucionados, a los que se utilizan en los secadores de pelo del mismo estilo), y que estos se han generado con paneles fotovoltaicos, es decir que para su creación necesitan tan solo la energía que proviene del sol.
- Ahorro de combustible: Los motores de ionización liberan energía que reduce muchísimo el consumo de combustible, de modo que quien sabe si estos podría tener algún tipo de aplicación futura en nuestras vidas.
Desventajas de la energía iónica
- Poco conocimiento y/o experiencia: La energía de ionización sigue siendo un tipo de energía por descubrir en lo que a usos reales y funciones más específicas se refiere.
- La ausencia de una energía estable: Esta energía no es del todo fiable, de modo que no podemos quedarnos con la idea de que a la larga se vaya a aplicar en usos cotidianos.
- Costosa de generar: Esta energía es bastante costosa de generar por su poca experiencia del manejo que se tiene con ella.
Energía de ionización ejemplos
- Hidrógeno (H) - 13.6
- Helio (He) - 24.59
- El boro (B) - 8.3
- Carbono (C) - 11.26
- Nitrógeno (N) - 14.53
- Oxygen (O) - 13.62
- Sodio (Na) - 5.14
- Aluminum (Al) - 5.99
- Cloro (Cl) - 12.97
- El calcio (Ca) - 6,11
Todos estos valores, sin embargo, son solo para el primer nivel de ionización. Eso significa que para averiguar el IE del siguiente nivel, multiplique la energía de ionización de primer nivel de cada elemento por 96.4689. Continúe multiplicando los nuevos valores por ese número para cada IE correspondiente.
Energía Iónica para niños
- La energía de ionización es la energía mínima requerida para eliminar un electrón de un átomo o ion en la fase gaseosa.
- Las unidades más comunes de energía de ionización son los kilojulios por mol (kJ / M) o los voltios de electrones (eV).
- La energía de ionización exhibe periodicidad en la tabla periódica.
- La tendencia general es que la energía de ionización aumente el movimiento de izquierda a derecha en un período de elemento. Moviéndose de izquierda a derecha a lo largo de un período, el radio atómico disminuye, por lo que los electrones son más atraídos hacia el núcleo (más cercano).
- La tendencia general es que la energía de ionización disminuya el movimiento de arriba a abajo hacia abajo en un grupo de tablas periódicas. Al mover hacia abajo un grupo, se agrega un shell de valencia. Los electrones más externos están más alejados del núcleo con carga positiva, por lo que son más fáciles de eliminar.
Maquetas del enlace ionico
A continuación te voy a mostrar algunas maquetas del enlace ionico que puedes hacer fácilmente con solo las imágenes te puedes ir haciendo una idea y crear tu maqueta estupenda.



Propiedades periodicas de la energia de ionizacion
Lo que es más destacado de las propiedades periódicas de los elementos se observa en un incremento de las energías de ionización cuando miramos la tabla periódica de izquierda a derecha, lo que se supone que es un incremento asociado de la electronegatividad, como una contracción del tamaño atómico y aumento del número de electrones ...
Tipos de enlace y electronegatividad
Covalente puro.
Es aquel que se da entre dos átomos que poseen exactamente la misma electronegatividad
pero todo esto se trata de un enlace de compartimiento de electrones entre dos o más átomos que esten en el mismo elemento. La diferencia de electronegatividades entre estos elementos será por esto de CERO.
COVALENTE NO POLAR
Cuando la electronegatividad de los compuestos que se unen son prácticamente cuantitativamente iguales, o mucho mas cercanos (ejp: O=O), debido a esto los electrones se mantienen cerca de los dos núcleos de forma que no existe un extremo que sea más polar que otro.
 Todo lo que siempre quisiste saber sobre la Energia Geotermica
Todo lo que siempre quisiste saber sobre la Energia GeotermicaCOVALENTE NO POLAR
Cuando la electronegatividad de los compuestos es cuantitativamente diferente, porque los electrones se mantendrán siempre cerca del núcleo más electronegativo por mayor tiempo. Por ello se pueden definir un polo negativo (con mayor numero de electrones) y un polo positivo (mucho menor) por ejemplo: O-H
Características de los enlaces ionicos:
- No forman moléculas reales, existe como un agregado de aniones (iones negativos) y cationes (iones positivos).
- Está formado por metal + no metal.
- Los metales entregan electrones formando cationes, los no metales solo aceptan electrones formando aniones.
- Los enlaces resultantes son de alguna interacción entre los metales de los grupos I y II y los no metales de los grupos VI y VII.
- Sus enlaces son bastantes fuertes (ya que depende fuertemente de la naturaleza de los iones).
Como se forman los enlaces ionicos
Este enlace se forma cuando los átomos de elementos metálicos (especialmente los situados más a la izquierda en la tabla periódica -períodos 1, 2 y 3) se encuentran con átomos que no son metálicos (los elementos situados a la derecha en la tabla periódica -especialmente los períodos 16 y 17).
En este caso los átomos del metal dan electrones a los átomos del no metal, transformándose en iones positivos y negativos, respectivamente.
Asi se define Electronegatividad
Definimos electronegatividad como un elemento que tiene la capacidad de traer hacia si los electrones, cuando se fomar una parte de un compuesto. Si un atomo tiene bastante tendencia a atraer electrones se dice que esto es porque es muy electronegativo.
Variación de las propiedades periódicas de los elementos
Los elementos cuando están en su configuración electrónica muestran una variación periódica al aumentar el número atómico. Entonces también presentan algunas variaciones en sus propiedades físicas y en las químicas.
Que son las propiedades periodicas de los elementos
Las propiedades periódicas de los elementos, son las características propias que tienen dichos elementos que varían de acuerdo a su posición en la tabla periódica, ósea dependiendo de su número atómico.
Las propiedades periódicas que existen son: electronegatividad, radio atómico, electropositividad, potencial de ionización, afinidad electrónica, la densidad atómica, temperatura de fusiónel, volumen atómico y temperatura de ebullición.
Calcular energia de ionizacion
Aprende a calcular la energía de ionización con este excelente vídeo.
¿Por que la energia de ionizacion es una propiedad periodica?
Esto es porque la energía de ionización es una propiedad de los elementos que representa la energia minima que se debe suministrar a un átomo que esta en estado gaseoso para así poder arrancar un electron de su capa de valencia.
Es denominada propiedad periódica debido a que varía dependiendo del lugar donde se encuentre este elemento en la tabla periódica, lo que permite también tener una idea de la energía de ionización de cierto elemento respecto a otros en la tabla dependiendo de su posición.
 Energía Hidráulica
Energía HidráulicaPorque la energía de ionización aumenta a lo largo de un periodo y disminuye cuando se va bajando en un grupo?
Esto sucede porque entre mayor sea la atracción ejercida a los electrones sera mucho mas difícil de arrancarlos del átomo en pocas palabra, necesitaremos mas energía para poder arrancarlo ya que cuando esta arriba necesitamos mas energía para arrancarlos átomos y a medida que baja de un grupo se necesitara menos por esta razon es que baja. Por esto se hace mayor cuando sube y disminuye cuando se baja.
¿Diferencia entre energía de ionización y potencial de ionizacion?
No existe ninguna diferencia ya que tanto como energía de ionización y potencia de ionización son los mismos siempre sera la cantidad mínima de energía necesaria para quitarle a un electrón un átomo.
Ionización de los átomos
Cuando un átomo gana un electrón, generalmente se libera energía. Esta energía se llama la afinidad electrónica de esa especie atómica. Los átomos que tienen una gran afinidad electrónica son más propensos a ganar un electrón y formar iones negativos.
La pérdida de un electrón de un átomo requiere una entrada de energía. La energía necesaria para eliminar un electrón de un átomo neutro es la energía de ionización de ese átomo. Es más fácil eliminar electrones de átomos con una pequeña energía de ionización, por lo que formarán cationes con más frecuencia en las reacciones químicas . Los metales tienden a tener una energía de ionización más pequeña, y los metales alcalinos (con su único electrón de valencia) tienen la energía de ionización más baja como grupo. Por lo tanto, la mayoría de las veces encontramos metales alcalinos como iones positivos en compuestos químicos, como el catión de sodio Na+ En sal de mesa, NaCl.
La energía de ionización también está relacionada con la función de trabajo de un metal, la energía mínima necesaria para expulsar electrones de una superficie metálica. La función de trabajo de un metal es importante en la electrónica y en la creación de instrumentos científicos como los cañones de electrones. Lea más sobre las funciones de trabajo y el efecto fotoeléctrico sobre los metales aquí.
Las tendencias en la energía de ionización y la afinidad electrónica, combinadas con los efectos de la estructura electrónica de un átomo, influyen en el tipo y la fuerza de los enlaces químicos que se forman entre los átomos.
Imagenes de energia ionica





 Energía Interna
Energía InternaDeja una respuesta

Existen en la actualidad empresas que atraves de las energia Iónica produzcan electricidad tal como la usamos.